Лаборатория химии диазосоединений (№ 6)

- Химия алифатических и ароматических диазосоединений.
- Химические превращения донорно-акцепторных циклопропанов и стирилмалонатов под действием кислот Льюиса.
- Химия 1,2-цвиттер-ионных интермедиатов, генерируемых в присутствии галогенидов галлия.
- Производные (2-фтораллил)пиридиния в качестве нового типа реагентов для процессов Pd-катализируемого фтораллилирования.
- Создание методологии контролируемых карбокатионных превращений, инициируемых «суперэлектрофильными» кислотами Льюиса, для дизайна новых лекарственных препаратов.
- Электронодефицитные циклогептатриены и их антиароматические анионы: строение, свойства и использование в синтезе карбо- и гетероциклических соединений.
- Создание технологичных методов циклопропанирования непредельных соединений.
✓ Открыта новая трехкомпонентная реакция β-стирилмалонатов с ароматическими или алифатическими альдегидами в присутствии алкоксиалюминийдихлорида, RСН2OAlCl2, приготовленного окислением EtAlCl2 при доступе воздуха или при смешивании эквимольных количеств AlCl3 с первичным или вторичным спиртом. В результате данного каскадного процесса, включающего α-CH-активацию алкоксида и вовлечение в циклизацию фрагмента –CH–O– алюминийорганического соединения, с выходами до 80% получен широкий ряд замещенных дигидро-2H-пиран-3,3(4H)-диэфиров. На основе изотопо-меченых исходных субстратов, PhCH18O и CH3CD2OAlCl2, предложен механизм протекающих превращений.
✓ Предложен подход к синтезу семичленных систем путем удлинения цепи нуклеофильных пропенов и последующей 8π-электроциклизации. Каскадная реакция дает либо циклогептадиены, либо бициклогептены, которые образуются в результате 6π-электроциклизации промежуточного циклогептадиенильного аниона. Электроциклическая природа реакций замыкания кольца подтверждена расчетами DFT и DLPNO/CCSD(T). Высокоэлектронодефицитные циклогептатриены могут быть получены из циклогептадиенов или бициклогептенов путем окисления, протекающего в каскадной реакции или проводимого в виде отдельной стадии, с общим выходом до 73%. Стадия окисления проводилась посредством редко встречающегося катализируемого Cu(II) дегидрирования циклогептадиенов или бициклогептенов, и для нее был предложен механизм реакции. Получены также стабильные формально 8π-антиароматические циклогептатриенил-анионсодержащие соединения. Кроме того, показано, что индуцированное основанием ретро-[2+2]-циклоприсоединение к производному бициклогептена дает цианотетра(метоксикарбонил)циклопентадиенилцезий.
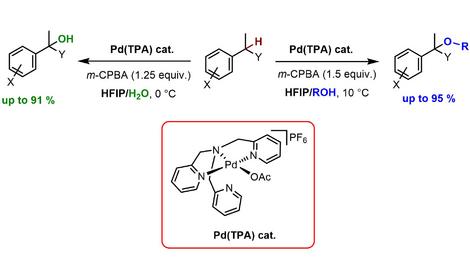
✓ Разработан эффективный двухстадийный синтетический подход к 2-фтораллиламинам, заключающийся в получении (2-фтораллил)пиридиний тетрафторборатов из легкодоступных гем-фторбромциклопропанов и их использовании как новых 2-фтораллильных электрофилов в Pd-катализируемом аллильном замещении. Синтезирован также новый боронилбориновый эфир, полученный путем гашения комплекса B2pin2/sec-BuLi-ат ангидридом трифторуксусной кислоты, который оказался эффективным для борилирования солей (2-фтораллил)пиридиния, высокочувствительных к основаниям.
✓ Разработаны и использованы в каталитической химии ДАЦ и родственных им субстратов катионные фталоцианиновые галлиевые катализаторы (RPcGa+) со слабокоординирующими анионами SbF6– и Sb2F11–. Впервые эти процессы были реализованы на примере реакций [3+2]-циклоприсоединения/аннелирования ДАЦ и изомерных им стирилмалонатов с различными альдегидами, а также некоторыми другими субстратами. Особенно активным оказался синтезированный нами катализатор tBu4(NO2)3PcGa+SbF6–, хорошо работающий даже с очень малоактивными D-A-циклопропанами с акцепторными заместителями (NO2, CF3, 2,6-Cl2) в арильном кольце. Полученные результаты демонстрируют высокий потенциал фталоцианиновых галлиевых катализаторов и их практическую полезность.
✓ Подробно изучены реакции стирилмалонатов с ароматическими альдегидами в присутствии кислот Льюиса и Бренстеда. Разработаны подходы к синтезу различных замещенных 5,6-дигидропиран-2-онов, инденов, арилсодержащих диенов и триенов, циклопентадиенов и полициклических лактонов с контролем хемо-, регио-, стерео- и диастереоселективности. Механизмы этих реакций были изучены с помощью многоядерных экспериментов ЯМР, мониторинга реакций в ампуле ЯМР и с использованием изотопной метки 18О.
Стирилмалонаты действительно оказались уникальными трехуглеродными синтонами, которые в ряде реакций проявляют иной тип реакционной способности по сравнению с изомерными 2-арилциклопропан-1,1-дикарбоксилатами.
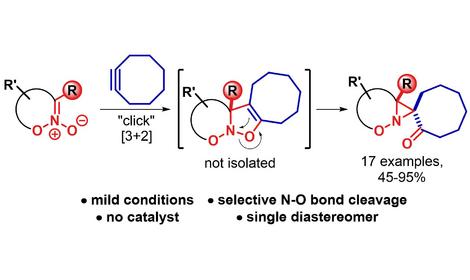
✓ Изучены реакции донорно-акцепторных циклопропанов и изомерных β-стирилмалонатов с конформационно нежесткими 1-азадиенами в присутствии кислот Льюиса. Основной задачей исследования являлось направление реакции по пути формального (4+2)-циклоприсоединения с полным вовлечением азадиеновой системы вместо известной методологии (3+2)-циклоприсоединения по одной связи C=N. Итогом работы стала разработка метода диастереоселективного синтеза замещенных транс,транс-тетрагидропиридинов в присутствии трифлатов скандия(III), олова(II) и хлорида галлия(III). Использование хлорида галлия в качестве кислоты Льюиса позволяет получить также минорный продукт формального (2+2+2)-циклоприсоединения, который представляет собой полностью 1,2,3,4,5,6-гексазамещенное производное циклогексана, образующееся с диастереоселективностью >30:1. Предложены соответствующие механистические и стереохимические модели протекания реакции.
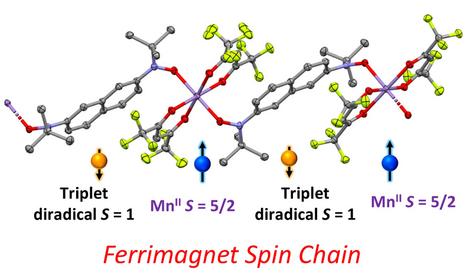
✓ Разработан новый подход к синтезу донорно-акцепторных хромофоров, содержащих гидразинилиденовые циклические акцепторные фрагменты, путем реакции литийорганических соединений с циклическими диазосоединениями. В отличие от классических подходов данный метод позволяет вводить в молекулу целевого хромофора тиофеновые фрагменты, что обеспечивает большую по сравнению с фениленовыми фрагментами планарность. Данный подход был успешно использован в синтезе гидразинилиденбарбитуровых и гидразинилидениндандионовых хромофоров, а также серии гидразоноциклопентадиенов с различными ароматическими и гетероциклическими заместителями. Полученные соединения проявили способность к интенсивному поглощению видимого света с максимумами абсорбции в области 373–562 нм и коэффициентами экстинкции до 36500 М−1⋅см−1. Важно, что ранее недоступные тиенилгидразоны проявили более длинноволновые максимумы абсорбции и более высокие коэффициенты экстинкции, чем обычные арилгидразоны.