Лаборатория направленной функционализации Органических молекулярных систем (№ 33)

- Химия донорно-акцепторных циклопропанов
- Новые перспективы использования илидов Кори – прерванные и расширенные версии реакции Кори-Чайковского, процессы двойного метиленового переноса
- Протонные ионные жидкости как реагенты тройного назначения в органической химии – реакционные среды, кислотные инициаторы, реагенты
- Превращения производных фурана в другие гетероциклические соединения
- Новые методологии синтеза редких классов функционализированных аза- и полиазагетероциклических соединений (в том числе полиазамакроциклов), основанные на химии амидов угольной кислоты, а также их тиоксо- и иминоаналогов
✓ Разработан метод синтеза бенз[b]азепинов, основанный на рециклизации 2,N-диарил-1-карбамоилциклопропанкарбоксилатов (26 примеров, выход до 92%). При использовании амидов на основе индолина и тетрагидрохинолина были получены трициклические аналоги биоактивных алкалоидов. Доказано, что реакция протекает с обращением конфигурации электрофильного атома углерода в трехчленном цикле, т.е. представляет собой первый пример 6-эндо-тет-циклизации и в целом первый пример эндо-тет-процесса, приводящий к образованию цикла. Полученные результаты показывают, что правила Болдуина для циклизаций требуют дополнения для процессов, включающих реакции малых циклов. Найдено, что диастереоселективность процесса зависит от времени реакции: через 1-2 часа заместители при атомах С(3) и С(5) в продукте расположены по одну сторону цикла (цис); если перемешивать реакционную смесь 1-2 дня, продукт имеет исключительно транс-расположение этих заместителей.
✓ Впервые осуществлена реакция рециклизации (реакция, в которой все атомы, образовывавшие исходный цикл, входят в состав нового цикла, для создания которого требуется образование по крайней мере одной новой связи) донорно-акцепторных циклопропанов, в которой в качестве экзоциклической группы принимает участие электрофильный sp3-атом углерода. Показано, что при действии бромида магния и основания донорно-акцепторный циклопропан, содержащий в качестве донора (гетеро)ароматический заместитель с бромометильной группой в орто-положении, перегруппировывается в 1,2-дигидронафталин-2,2-дикарбоксилат (или родственные соединения с двумя другими акцепторами). Полученные дигидронафталины превратили в мостиковые трициклические лактоны, представляющие интерес для фармакологии.
✓ Изучено взаимодействие донорно-акцепторных циклопропанов с 5-амино-1,3-диметилпиразолом и его производными. Показано, что в присутствии кислоты Льюиса 5-аминопиразолы ведут себя по отношению к циклопропанам как амбидентные нуклеофилы, образуя продукты алкилирования либо по атому С(4) пиразольного цикла, либо по экзоциклической аминогруппе. Определено влияние заместителей и условий проведение реакции на селективность процесса; найдены условия для селективного N-алкилирования. Показано, что некоторые циклопропаны могут образовывать исключительно продукты C-алкилирования в определенных условиях. При нагревании с кислотой продукты С-алкилирования были превращены в производные пиразоло[4,3-b]азепина, проявляющие высокое сродство по отношению к глюкокортикостероидным рецепторам, а продукты N-алкилирования – в производные 5-арил-1-(пиразол-3-ил)пирролидин-2-она.
✓ Разработана концепция использования протонных ионных жидкостей для проведения разнообразных реакций как веществ тройного назначения: растворитель, источник протона (общий кислотный катализ), реагент. Концепция продемонстрирована на примере тиоцианатов 1-метилимидазолия, триэтиламмония и тетраметилгуанидиния. Нагревание донорно-акцепторных циклопропанов в тиоцианате 1-метилимидазолия приводит к образованию 5-арил(алкенил)пирролидин-2-тионам, содержащим в положении 3 две акцепторные группы, в результате кислотно-катализируемого нуклеофильного раскрытия трехчленного цикла тиоцианат-ионом как N-нуклеофилом с последующей атакой малонильного фрагмента по атому углерода образовавшегося изотиоцианата. Показано, что после проведения реакции протонная ионная жидкость может быть регенерирована и использована повторно, причем выход продукта не снижается после проведения по крайней мере четырех регенераций. Для наиболее реакционноспособных субстратов выходы продуктов при использовании тиоцианата 1-метилимидазолия оказываются невысокими; эта проблема была решена использованием менее кислотного тиоцианата триэтиламмония. Полученные протонные ионные жидкости оказались эффективны также для раскрытия эпоксидов (атомом серы), превращения a-аминокислот в 2-тиоксоимидазолин-4-оны (через образование амида) и др. процессах.
✓ Тиоцианат-содержащие протонные ионные жидкости применены в качестве реагентов тройного действия (регенерируемый растворитель, источник протона — кислотный катализатор и нуклеофил) для раскрытия цикла донорно-акцепторных циклопропанов. Впервые продемонстрирована амбидентность тиоцианат-иона при раскрытии донорно-акцепторного циклопропанов на основе 1,4-индандиона как функция основания, образующего протонную ионную жидкость. В зависимости от используемой протонной ионной жидкости в результате домино реакции образуются либо 2-тиоксоспиро[пирролидин-3,2'-индан-1',3'-дионы] (продукт формального раскрытия циклопропана атомом азота тиоцианат иона с последующей внутримолекулярной атакой СН-кислотного атома по атому углерода изотиоцианата), либо тиено[2,3-c][2]бензазепины (продукты раскрытия малого цикла атомом серы и последующих вторичных реакций образовавшегося тиоцианата).
✓ Разработан стабильный, невзрывчатый, малогигроскопичный источник азид-иона, растворимый как в протонных, так и во многих апротонных органических растворителях — азид 4-(диметиламино)пиридиния. Показано также, что при использовании его раствора в протонных ионных жидкостях он выступает в качестве безопасного эквивалента токсичной и нестабильной азотистоводородной кислоты. Термохимическими методами показано, что данный азид разлагается с поглощением, а не с выделением энергии. Синтетическая значимость разработанного реагента продемонстрирована на примере реакций нуклеофильного раскрытия донорно-акцепторных циклопропанов и оксиранов, циклоприсоединения к нитрилам и изотиоцианатам. Для широкой серии донорно-акцепторных циклопропанов определена их относительная реакционная способность по отношению к этому реагенту.
✓ Предложен новая концепция получения разнообразных органических соединений — использование «расширенной» реакции Кори-Чайковского в дополнение к классическому варианту этой реакции и её «прерванной» версии. Эта концепция подразумевает превращение образующихся в реакции Кори-Чайковского трехчленных циклов без их выделения в более сложные продукты в результате домино-реакции или при добавлении к образовавшейся смеси новых реагентов, инициируя превращение «в одном реакторе». Предложенная концепция использована для превращения коммерчески доступных или легко синтезируемых халконов в бензаннелированные 2,8-диоксабицикло[3.2.1]октаны и в 2,3-дигидробензофураны.
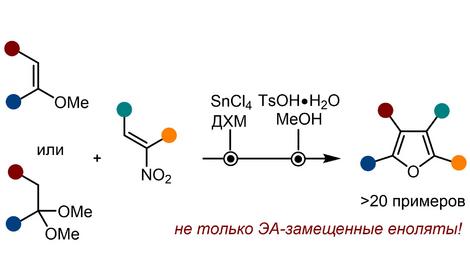
✓ Для нового метода синтеза 2,4-дизамещенных фуранов использована предложенная недавно концепция расширенной реакции Кори-Чайковского. Легко доступные b,b-дизамещенные a,b-ненасыщенные кетоны обрабатывали метилидом диметилсульфония. Образующийся при этом винилоксиран в условиях реакции немедленно перегруппировывается в дигидрофуран, ароматизация которого в результате отщепления одного из b-заместителей приводит к целевому 2,4-замещенному фурану. Разработанный подход позволяет синтезировать широкий круг 2,4-ди- и 2,3,4-тризамещённых фуранов, представляющих интерес как для фармакологии, так и для химии материалов.
✓ Разработан метод синтеза 3-(2-фурил)-1,3-ди(гет)арилпроп-2-ен-1-онов, основанный на окислительной рециклизации 3-(2-фурил)-1,3-ди(гет)арилпропан-1-онов, протекающий в результате окислительного раскрытия фуранового цикла с образованием ди(гет)арил-замещенных 2-ен-1,4,7-трионов с последующим образованием фурана из фрагмента насыщенного дикетона. В результате заместители, присутствовавшие в фурановом цикле, оказываются в боковой цепи, и наоборот.
✓ Окислительной перегруппировкой замещенных 2-(2-аминобензил)фуранов получены 2-(2-ацилвинил)индолы, которые далее использовались для получения различных замещенных индолов и карбазолов, в том числе структурных аналогов алкалоидов каулиндолов A–D. Показаны возможности расширения данного подхода для получения других типов гетероциклов.
✓ Показано, что гидразоны 4-(4-тиосемикарбазидо)бутан-2-онов подвергаются кислотно-промотируемой циклоолигомеризации с образованием новых 14-членных циклических бис(тиосемикарбазонов) и/или 28-членных циклических тетракис(тиосемикарбазонов). Определены факторы, влияющие на направление реакции, и условия, позволяющие селективно получать необычные циклы.
✓ Аналогичные 14-членные циклические бис(семикарбазоны) были получены из соответствующих 4-(3-оксобутил)семикарбазонов.
✓ Получено три новых тиосемикарбазона, наличие в которых ред-окс активного фенольного фрагмента позволяет рассматривать их как аналоги триапина. Эти лиганды стабильны при рН 7.4, но нестабильны в щелочной среде. В диметилсульфоксиде они существуют в виде смеси E- и Z-изомеров; предложен механизм E-/Z-изомеризации с инверсией при атоме азота, образующего иминную связь. Получены комплексы этих лигандов с хлоридом меди(II), их электрохимическое и спектроэлектрохимическое изучение подтвердили их ред-окс активность как в катодной, так и в анодной области потенциалов. Полученные комплексы показали важную антипролиферативную активность по отношению к раковым клеткам Colo205 и Colo320. Один из лигандов, как и его комплекс с медью продемонстрировал способность ингибировать mR2 рибонуклеотид редуктазу с той же активностью, что и триапин.
✓ Разработан метод синтеза соединений с беспрецедентным тетрациклическим скелетом, содержащим фрагмент тропана, пери-аннелированный к индольному ядру, на основе реакции 3-формилиндол-4-ил-замещенного донорно-акцепторного циклопропана с анилинами и другими первичными аминами. Продукты включают в себя сразу 4 известных фармакофора — тропан, индол, фрагменты b-аминокислоты и g-аминомасляной кислоты.
✓ Обнаружено, что взаимодействие 3-формилиндол-4-ил-замещенных донорно-акцепторных циклопропанов с бензиламинами и их гетероциклическими аналогами приводит к преимущественному образованию тетрациклов, изомерных «тропаноиндолам», полученным ранее в реакции этих циклопропанов с анилинами. Образование нового типа продуктов с ранее неизвестным скелетом объяснено атакой атома азота промежуточного имина на незамещенный атом углерода трехчленного цикла, что нехарактерно для донорно-акцепторных циклопропанов. Такое направление является следствием стереоэлектронных факторов в реакционной конформации, препятствующих сопряжению трехчленного цикла с индольным кольцом.
✓ Развивая исследования по синтезу новых пери-аннелированных индолов из 3-формилиндол-4-ил-замещенных донорно-акцепторных циклопропанов, изучена их реакция с гидразинами. Показано, что даже в отсутствии катализаторов эта реакция приводит к образованию производных [1,2]диазепино[4,5,6-cd]индола; соответствующие циклические карбогидразиды являются эффективными PARP ингибиторами и применяются в качестве антираковых агентов. Пост-модификацией полученных продуктов получены тетрациклические соединения с ранее неизвестным скелетом, являющиеся структурными аналогами ряда биоактивных веществ, а следовательно — перспективные для изучения их физиологической активности.
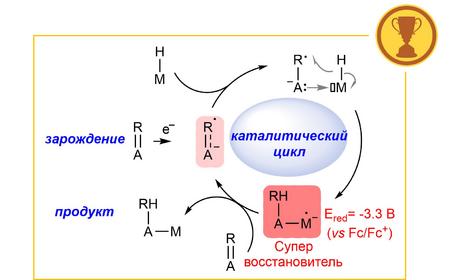
✓ В составе международной группы исследователей предложен принципиально новый способ активации донорно-акцепторных циклопропанов. Донорно-акцепторные циклопропаны, содержащие в качестве донора орто- или пара-гидроксиарильную группу, а также орто- или пара-тозиламино-замещенную арильную группу при действии основания подвергаются депротонированию и изомеризации образующегося аниона в производное орто- или пара-хинонметида (азахинонметида). Нуклеофильная частица, присутствующая в реакционной среде, атакует хинонметид с восстановлением ароматичности бензольного цикла с образованием продукта формального раскрытия циклопропана данным нуклеофилом. Использование в этой реакции в качестве нуклеофила илидов серы позволяет осуществлять процесс (4+1)-аннелирования с образованием производных 2,3-дигидробензофурана, что имеет важное значение для получения различных фармпрепаратов и соединений с доказанной физиологической активностью, еще не получивших разрешение на использование в качестве лекарств.
✓ В результате совместного исследования с сотрудниками МГУ и НМИЦ ДГОИ им. Дм. Рогачева разработан предельно простой метод синтеза g-арил-g-аминомасляных кислот, структурных аналогов важнейшего нейромедиатора в организме человека, а также соответствующего винильного производного — мощного противоэпилептического средства вигабатрина.
✓ В ходе совместного исследования с сотрудниками МГУ изучено инициируемое кислотами Льюиса взаимодействие (гет)арилзамещенных донорно-акцепторных циклопропанов со стиролами. В условиях инициирования процесса хлоридом олова(IV) такое взаимодействие протекает по двум альтернативным направлениям с образованием замещенных циклопентанов (продуктов (3+2)-циклоприсоединения) и замещенных инданов или их гетероаналогов (продуктов (3+2)-аннелирования). Хемоселективность взаимодействия контролируется рядом факторов: природой реагирующих соединений и инициатора, условиями проведения реакции.
✓ Разработан препаративный синтез 14-членных и 21-членных азамакроциклов реакциями циклодимеризации (циклотримеризации) легко доступных тиосемикарбазидов.
✓ В составе международной группы исследователей описаны синтез и физико-химические характеристики комплексов меди(II) с морфолин-замещенным тиосемикарбазоном 2-формилпиридина как потенциальных противораковых агентов. Найдено, что положение морфолинометильного заместителя в пиридиновом цикле оказывает заметное влияние на противораковую активность как самих лигандов, так и их комплексов с медью(II). Предложен механизм антипролиферативной активности изученных соединений.
✓ В составе международной группы исследователей описан синтез новых 14-членных бис(тиосемикарбазидов) и бис(изотиосемикарбазидов), а также их комплексов с никелем(II). Продукты охарактеризованы широким спектром физико-химических исследований. Показано, что никелевые комплексы активны как электрокатализаторы в реакция выделения кислорода при электролизе воды в щелочной среде, проявляя при этом высокую стабильность в условиях реакции, что позволяет утверждать о перспективах дальнейшей разработки использования таких соединения в коммерческих системах.
✓ Протонные ионные жидкости тройного назначения использованы в качестве растворителя, кислотного катализатора и источника нуклеофила (тиоцианат-иона) для хемодивергентного превращения дигидроимидазолонов в 2-тиоксогексагидро-5H-имидазо[4,5-d]оксазол-5-оны и тетрагидро-2H-имидазо[4,5-d]тиазол-2,5(3H)-дионы. Важной особенностью этого процесса является переключение его хемоселективности простым изменением температуры реакции при прочих равных условиях; это позволило селективно получать оба типа продуктов. Простая водная обработка реакционной смеси позволила получить твердые бициклические продукты в чистом виде экологически безопасным способом.
✓ Многоцелевые тиоцианат-содержащие протонные ионные жидкости использовались совместно в качестве растворителя, кислотного катализатора Брёнстеда и источника нуклеофила для превращения 4,5-дигидрокси-4,5-диарилимидазолидин-2-(ти)онов в имидазо[4,5-d]оксазолтионы и имидазо[4,5-d]тиазолоны. Ключевым преимуществом этого процесса является переключение хемоселективности путем настройки электронодонорной природы арильных заместителей при тщательном контроле температуры реакции. В случае неактивированных аренов оксазолтион был вынужден перегруппироваться в тиазолон в новой сильнокислотной протонной ионной жидкости, трифлате 1-метилпиразолия. Простая в эксплуатации экспериментальная установка дополняется экологически чистой процедурой водной обработки/фильтрации, обеспечивающей получение чистых кристаллических продуктов.
✓ Тиоцианатсодержащие протонные ионные жидкости (ПИЖ) ранее зарекомендовали себя как полезные реагенты для проведения различных химических превращений. Принципиально новая концепция многоцелевого применения этих ПИЖ открывает новые возможности в органическом синтезе. Однако их безопасность до сих пор не была до конца изучена. В данной работе проведено систематическое исследование цитотоксичности ряда синтетически ценных тиоцианатсодержащих ПИЖ в отношении нормальных фибробластов дермы человека (DF-1) и клеток эмбриональной почки человека (HEK293T).
В частности, изучено влияние аниона на цитотоксичность ПИЖ двойного назначения на основе триэтиламина. Исследование маркеров клеточных повреждений позволило получить дополнительную информацию о механизмах цитотоксичности ПИЖ.
✓ В исследовании, выполненном совместно с учеными Приволжского (Казанского) федерального университета, изучены термохимические свойства восьми тиоцианатных (SCN) протонных ионных жидкостей или расплавленных солей с различной структурой катионов: тиоцианатов 1-метилимидазолия ([MIm]), 1-этилимидазолия ([EIm]), н-бутиламмония ([BA]), триэтиламмония ([TEA]), диизопропилэтиламмония ([DIPEA]), гуанидиния ([Gu]), 1,1,3,3-тетраметилгуанидиния ([TMG]) и тиазолия ([Tz]). Термическая стабильность исследована методом термогравиметрического анализа (ТГА) в динамическом (нагрев от 30 до 500 °C) и изотермическом (выдержка при 120 °C) режимах.
В динамических экспериментах показано, что стабильность возрастает в ряду [Tz][SCN] < [BA][SCN] < [TEA][SCN] ≈ [DIPEA][SCN] < [MIm][SCN] ≈ [EIm][SCN] < [TMG][SCN] ≈ [Gu][SCN]. Обнаружено, что [Tz][SCN] и [DIPEA][SCN] начинают разлагаться ниже температуры плавления. Изотермические эксперименты показали долговременную термическую стабильность [MIm][SCN], [EIm][SCN], [TEA][SCN], [TMG][SCN] и [Gu][SCN] в широком диапазоне температур выше температуры плавления, что делает их перспективными для экстракции, разделения, каталитических реакций и других промышленных и лабораторных применений. Полученные результаты могут быть использованы для выбора оптимальных условий проведения этих процессов, а также для регенерации ионных жидкостей.
✓ Протонные ионные жидкости имеют многочисленные перспективные применения в качестве растворителей и более просты и менее затратны в синтезе, чем апротонные ионные жидкости. В работе, выполненной совместно с учеными Приволжского (Казанского) федерального университета, исследованы сольватационные свойства протонных ионных жидкостей на примере трех триэтиламмониевый солей: ацетата, трифторацетата и трифлата. Кроме того, они были охарактеризованы с помощью анализа ТГ/ДСК и низкотемпературной ДСК с целью определения температуры жидкого диапазона. В этих жидкостях были измерены предельные коэффициенты активности алканов, алкенов, ароматических углеводородов, циклоалканов, циклогексена и тиофена при 298,15 К. Наблюдалась более высокая растворимость углеводородов в триэтиламмониевых солях, чем во многих апротонных и нескольких изученных протонных ионных жидкостях. Селективность триэтиламмонийтрифлата при разделении н-гексана и бензола выше, чем у сульфолана и N-метил-2-пирролидинона, используемых в промышленных процессах экстракции.
✓ В исследовании, выполненном совместно с сотрудниками Северо-Осетинского, Пермского и Ростовского (ЮФУ) университетов, изучена реакционная способность различных фуранов по отношению к 2-азидобензальдегидам, гетероциклическим азидоальдегидам и замещенным 2-азидобензиловым спиртам для синтеза производных 2-(2-азидобензил)фурана. Результаты показывают замечательную совместимость азидной группы с типичными условиями реакции Фриделя-Крафтса. Продемонстрировано, что эти производные могут быть эффективно синтезированы, используя последовательность диазотирование/азидирование из 2-(2-аминобензил)фуранов, содержащих электронодонорные заместители. Кроме того, разработана синтетическая методология для получения 2-(2-ацилвинил)индолов, включающая термическое образование нитренов для инициирования раскрытия фуранового кольца. Широкая применимость и высокая эффективность предложенного метода, использующего легкодоступные исходные материалы, подчеркивают его потенциал как универсального синтетического инструмента.
✓ В исследовании, проведенном совместно с Пермским государственным университетом, сообщается о домино-реакции 2-(2-ацилвинил)индолов, а также соответствующих пирролов со стирилсульфониевыми солями в мягких условиях, приводящей к образованию аналогов циклопропамитозена с высокими выходами и полной диастереоселективностью. Широкий спектр (E)-β-гетарил-α,β-ненасыщенных кетонов был успешно использован для синтеза потенциально биоактивных циклопропа[3,4]пирроло[1,2-a]индолов и родственных им циклопропа[a]пирролизинов, что демонстрирует универсальность разработанного метода. Напротив, (Z)-изомеры субстратов не дают производных циклопропамитозена, а подвергаются циклопропанированию по терминальной метильной группе.