Лаборатория ароматических азотсодержащих соединений (№ 18)

- Развитие фундаментальных основ химии ароматических и азотсодержащих гетероциклических нитросоединений с целью создания методологий синтеза на их основе новых потенциальных компонентов энергетических материалов, биологически активных веществ, а также реагентов — химических строительных блоков.
✓ The discovery of novel explosophoric building blocks for the construction of energetic compounds is extremely rare. Here, based on the comparative experimental properties and computational analysis of compounds where nitroaryl backbones were bonded with various nitrogen/oxygen-rich groups, it is shown that compounds having the azasydnone group possess higher density, detonation performance and thermal stability than their corresponding nitro, azido and tetrazole-analogs. All of these properties, as well as the oxygen balanced content of the “green” nitrogen rich endothermic unit make them an attractive explosophoric building block in the field of energetic materials chemistry.
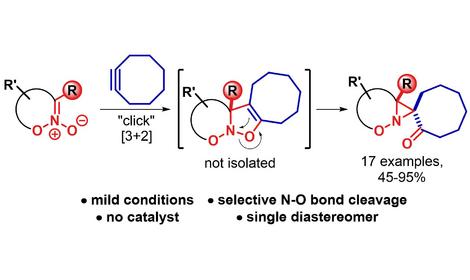
✓ The first example of functionalization of mesoionic 3-R-1,2,3,4-oxatriazol-5-ones and 3-substituted-1,2,3,4-oxatriazol-5-imines (azasydnones and azasydnonimines, respectively) by the electrophilic reaction without destruction of the oxatriazole ring is reported. Nitration of a range of aryl derivatives bearing various electron donating and withdrawing substituents at the ortho-, meta- and para-positions using HNO3/H2SO4 mixtures has been assessed in order to develop an approach for the synthesis of corresponding nitroaryl derivatives. Whereas nitration occurs meta to the azasydnone ring, the regioselectivity of the electrophilic substitution can be affected by the nature of the substituent attached to the aryl ring, and a variety of polyfunctionalized derivatives can be readily accessed by using this methodology, which may have applications in the targetoriented synthesis. The reactivity, synthesis, and structure of the mesoionic 3-substituted-1,2,3,4-oxatriazole derivatives described here provide interesting new information on this known but poorly understood heterocycle.
Reaction with nucleophiles of a range of 3-arylazasydnones bearing chloro and nitro substituents at the various positons at the phenyl ring using ammonia, primary and secondary amines and azide ion has been assessed in order to develop methodology for the synthesis of corresponding aminophenyl azasydnone derivatives. It has been shown that a nitrogen nucleophile can cause (i) an SNAr reaction when a halogen or the azasydnone moiety itself can be a leaving group; (ii) the azasydnone ring-opening leading to the formation of aryl azides or azocarboxamides. The observed reactivity of the substrates is discussed in the context of the substituent effect and the nature of the nucleophile.
✓ There is a need for dense energetic oxidizers whose composition is restricted to carbon, hydrogen, nitrogen and oxygen atoms as chlorine-free alternative to current oxidizers of energetic materials such as explosives, propellants and pyrotechnics. High nitrogen heterocyclic frameworks containing trinitromethyl units are an attractive and increasingly important class of oxygen-rich compounds. Herein, for the first time, a synthetic method has been developed for the preparation of a new (pyrazole-3-yl)furazan framework. From this framework, 3-nitro-4-(4-nitro-1-(trinitromethyl)-1H-pyrazol-3-yl)furazan and 3-(3,4-dinitro-1-(trinitromethyl)-1H-pyrazol-5-yl)-4-nitrofurazan have been produced. The combination of positive enthalpy of formation, high density, favorable physical and thermal properties, and reasonable sensitivity with the promising theoretical energetic performance of these oxygen-rich compounds offers materials not only of fundamental interest, but also for potential practical applications, for example, as promising candidates to new environmentally benign rocket propellants.
✓ High-nitrogen-content compounds have attracted great scientific interest and technological importance because of their unique energy content, and they find diverse applications in many fields of science and technology. Understanding of structure–property relationship trends and how to modify them is of paramount importance for their further improvement. Herein, the installation of oxygen-rich modules, C(NO2)
✓ Предложен удобный метод синтеза новых тиазоло[4,5-b]пиридинов, конденсированных с триазольным или пиримидиновым циклом. Реакции замещенных 3-нитро-2-хлорпиридинов с 1,3-(S,N)-бинуклеофилами (1,2,4-триазол-5-тиолами, 4-оксопиримидин-2-тионами) в присутствии основания протекают через нуклеофильное замещение атома хлора, перегруппировку Смайлса S-N типа с последующим нуклеофильным замещением нитрогруппы. Реакции с пиримидин-2-тионами проводили как “one-pot” процесс, в случае триазол-5-тиолов выделение промежуточных продуктов замещения оказалось предпочтительным.
✓ Синтезирован ряд ранее неизвестных 6-R-изоксазоло[4,3-b]пиридинов и изучены их реакции с нейтральными С-нуклеофилами (1,3-дикарбонильными соединениями, π-избыточными (гет)аренами, диенами). Обнаружено, что скорость реакций зависит от природы заместителя 6-R. Наиболее реакционноспособные 6-нитроизоксазоло[4,3-b]пиридины способны присоединять С-нуклеофилы в отсутствии основания в мягких условиях. Показано, что эти соединения гладко вступают в реакции [4+2]-циклоприсоединения по ароматическим связям C=C(NO2) пиридинового кольца, что указывает на суперэлектрофильную природу 6-R-изоксазоло[4,3-b]пиридинов.
✓ Синтезирована серия 3-R-5-нитропиридинов и изучены их реакции с различными типами нуклеофилов. Результат реакций зависит от природы нуклеофила: в случае анионных O-, N- и S-нуклеофилов наблюдается неизвестное ранее нуклеофильное замещение неактивированной нитрогруппы, в то время как С-нуклеофилы присоединяются в положение 2 или 4 пиридинового цикла с образованием продуктов деароматизации.
✓ Разработаны простые и эффективные способы получения 2-R-6,8-динитро[1,2,4]триазоло[1,5-a]пиридинов на основе коммерчески доступных исходных соединений. Указанные бициклические производные образуются с высокими выходами в мягких условиях за счет циклизации соответствующих 3,5-динитропиридин-2-ил гидразидов или 3,5-динитропиридин-2-ил гидразонов альдегидов с последующей перегруппировкой Димрота. Другим подходом к целевым динитро[1,2,4]триазоло[1,5-a]пиридинам является арилирование 5-арилтетразолов 3,5-динитро-2-хлорпиридином и последующая термическая рециклизация.
✓ Ряд 4-нитробензофуроксанов изучен в реакциях [3+2]-циклоприсоединения с N-бензилазометинилидом. Обнаружено, что результат реакций зависит от природы заместителя в положении 7: при R = H и SR’ были выделены продукты двойного циклоприсоединения диполя, в то время как в случае R = CH3, OR’ и NR’R” единственными продуктами были тетрагидроизоиндолы, конденсированные с фуроксановым циклом. Таким образом, разработан эффективный хемоселективный метод синтеза производных конденсированных с одним или двумя пирролидиновыми циклами.